1. 전기? 분자? ¶
쌍극자,dipole의 양쪽 끝 전하량 Q와 전하 간 거리 r의 곱으로 정의

단위: D (debye)
벡터량
쌍극자 모멘트 값이 클수록 극성이 강함
1 D = 3.336×10-30 C m (coulomb meter)
극성,polarity과 비례벡터량
쌍극자 모멘트 값이 클수록 극성이 강함
무극성 분자는 쌍극자 모멘트 합이 0
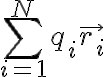 란 식이 있는데 CHK
란 식이 있는데 CHK
Q: 각 원자에 대해 계산해서?
쌍극자모멘트 = 화학적 관점의 서술
https://nate9389.tistory.com/1330?category=1024960 에서 2. 쌍극자 모멘트
{
여기에 의하면 물리/화학에서 방향이 반대라고?
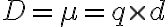
q = 원자의 전하 세기, d = 전하 간 거리
분자의 쌍극자 모멘트 : 분자 내 모든 결합의 쌍극자 모멘트를 모두 더한 값
}
https://nate9389.tistory.com/1330?category=1024960 에서 2. 쌍극자 모멘트
{
여기에 의하면 물리/화학에서 방향이 반대라고?
q = 원자의 전하 세기, d = 전하 간 거리
분자의 쌍극자 모멘트 : 분자 내 모든 결합의 쌍극자 모멘트를 모두 더한 값
}
3. 결합쌍극자모멘트,bond_dipole_moment ¶
// QQQ 바로 위 section과의 관계?? 정확히
화학에서는 (쌍극자모멘트,dipole_moment가) 결합 쌍극자 모멘트(bond dipole moment)의 뜻인 경우가 많단다
분자,molecule의 이온성(? 잘 안 쓰이는 단어인데 see 이온성
이온성  이온성 ...
이온성 ... ![[https]](/123/imgs/https.png) 이거 맞는지? chk)과 전기음성도,electronegativity 차이를 측정하는 데 유용. (wpko)
이거 맞는지? chk)과 전기음성도,electronegativity 차이를 측정하는 데 유용. (wpko)
"결합 쌍극자 모멘트(bond dipole moment)는 ..... 화학에서 쓸 때는 간단히 쌍극자 모멘트(dipole moment)라 부르기도 한다." (wpko)
화학결합,chemical_bond의 극성,polarity을 나타내는 척도이며,분자,molecule의 이온성(? 잘 안 쓰이는 단어인데 see
![[https]](/123/imgs/https.png) 이거 맞는지? chk)과 전기음성도,electronegativity 차이를 측정하는 데 유용. (wpko)
이거 맞는지? chk)과 전기음성도,electronegativity 차이를 측정하는 데 유용. (wpko)

![[http]](/123/imgs/http.png)