Johannes Rydberg: 스웨덴 물리학자 (1854 – 1919)
1. 뤼드베리 공식 Rydberg formula ¶
수소에서만 성립?
moved from spectrum
{
Lyman series (라이먼 계열)
\quad(n=2,3,4,\cdots))
Balmer 계열
\quad(n=3,4,5,\cdots))
Paschen 계열
Brackett 계열
Pfund 계열
Humphreys 계열
{
Lyman series (라이먼 계열)
Brackett 계열
Pfund 계열
Humphreys 계열
종합하면,
QQQ aka Rydberg_equation ? chk ... https://everything2.com/title/Rydberg equation
2. 뤼드베리 상수 Rydberg constant ¶
기호
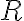
 for heavy atoms
for heavy atoms
 for hydrogen
for hydrogen
moved from spectrum
{
수소,hydrogen의 경우임?
{
수소,hydrogen의 경우임?
수소를 강조하기 위해  로 표기하기도
로 표기하기도
 는 뭐임?
는 뭐임?
R = 1.097… × 107 m-1
R = 1.097… × 10-2 nm-1 CHK
}R = 1.097… × 107 m-1
R = 1.097… × 10-2 nm-1 CHK
보어 모델에서 수소 원자 내 전자 에너지는
)
여기서
 : 뤼드베리 상수
: 뤼드베리 상수
n=1: 가장 안정, 바닥 상태/바닥 준위 (ground state/level)
n=2, 3, …: 들뜬 상태/들뜬 준위 (excited state/level)
n이 무한대가 되면 전자 에너지는 0이 됨: 이것은 자유전자가 되었음을 뜻함.
n=2, 3, …: 들뜬 상태/들뜬 준위 (excited state/level)
n이 무한대가 되면 전자 에너지는 0이 됨: 이것은 자유전자가 되었음을 뜻함.

