Heisenberg uncertainty principle
from https://terms.naver.com/entry.naver?docId=3568644&cid=58941&categoryId=58960 물리산책: 불확정성의 원리
QM에서 입자,particle는 파속,wave_packet을 이용해 나타낸다.
불확정성의 원리:
입자는 파속,wave_packet(이하 wp) 안의 어느 곳에 있게 되는데,
wp의 너비가 좁으면 위치에 대한 불확실성이 작아지고, 반대로
wp의 너비가 커지면 위치에 대한 불확실성이 커진다.
좁은 너비를 가지는 wp를 만들기 위해서는, (위치를 확실히 하기 위해서는?) 다른 진동수,frequency를 가지는 더 많은 파동을 더해야 한다.
입자의 운동량은 진동수에 비례하고 따라서 파장,wavelength에 반비례한다.
그러므로 좁은 너비를 가지는 wp을 만들기 위해 다른 진동수를 가지는 많은 파동을 더하게 되면 운동량의 불확실성이 커진다.
다시 말해 위치측정오차를 줄이면 운동량측정의 오차가 증가한다. (vice versa?) 이것이 위치와 운동량 사이에 존재하는 불확정성이다. Heisenberg는 위치 오차와 운동량 오차,error의 곱은 일정한 값 이상일 수 밖에 없음을 수학적으로 증명했다. 식으로는
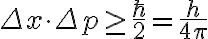
이 원리 때문에 위치와 운동량을 동시에 정확하게 측정,measurement하는 것은 불가능하다.
불확정성의 원리:
입자는 파속,wave_packet(이하 wp) 안의 어느 곳에 있게 되는데,
wp의 너비가 좁으면 위치에 대한 불확실성이 작아지고, 반대로
wp의 너비가 커지면 위치에 대한 불확실성이 커진다.
좁은 너비를 가지는 wp를 만들기 위해서는, (위치를 확실히 하기 위해서는?) 다른 진동수,frequency를 가지는 더 많은 파동을 더해야 한다.
입자의 운동량은 진동수에 비례하고 따라서 파장,wavelength에 반비례한다.
그러므로 좁은 너비를 가지는 wp을 만들기 위해 다른 진동수를 가지는 많은 파동을 더하게 되면 운동량의 불확실성이 커진다.
다시 말해 위치측정오차를 줄이면 운동량측정의 오차가 증가한다. (vice versa?) 이것이 위치와 운동량 사이에 존재하는 불확정성이다. Heisenberg는 위치 오차와 운동량 오차,error의 곱은 일정한 값 이상일 수 밖에 없음을 수학적으로 증명했다. 식으로는
양자역학,quantum_mechanics에서 ..TBW
위치의 불확정성 Δx
운동량의 불확정성 Δp
운동량의 불확정성 Δp
Δx Δp ≥ h
에너지의 불확정성 ΔE
측정 시간 Δt
측정 시간 Δt
ΔE Δt ≥ h
TOSEARCH h가 아니라 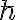 인가?
인가?
// tmp from 김성호 https://youtu.be/BSTQphLVJ-c?t=306
{
입자의 위치와 운동량은 일정 수준의 정확도 이상으로 동시에 측정할 수 없다.
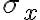 : 측정된 위치,position의 표준편차,standard_deviation
: 측정된 위치,position의 표준편차,standard_deviation
 : 측정된 운동량,momentum의 표준편차
: 측정된 운동량,momentum의 표준편차
}
{
입자의 위치와 운동량은 일정 수준의 정확도 이상으로 동시에 측정할 수 없다.
}
tmp links ko
http://blog.naver.com/cj3024/221234239778
tmp videos
https://www.youtube.com/watch?v=MBnnXbOM5S4 - 3b1b - The more general uncertainty principle, beyond quantum
http://blog.naver.com/cj3024/221234239778
tmp videos
https://www.youtube.com/watch?v=MBnnXbOM5S4 - 3b1b - The more general uncertainty principle, beyond quantum
Twins:
![[https]](http://tomoyo.ivyro.net/123/imgs/https.png) 물리학백과: 불확정성원리(https://terms.naver.com/entry.naver?docId=5810582&cid=60217&categoryId=60217)
물리학백과: 불확정성원리(https://terms.naver.com/entry.naver?docId=5810582&cid=60217&categoryId=60217)
![[https]](http://tomoyo.ivyro.net/123/imgs/https.png) 물리산책: 불확정성의 원리(https://terms.naver.com/entry.naver?docId=3568644&cid=58941&categoryId=58960)
물리산책: 불확정성의 원리(https://terms.naver.com/entry.naver?docId=3568644&cid=58941&categoryId=58960)
https://everything2.com/title/Heisenberg Uncertainty Principle (long)
![[https]](http://tomoyo.ivyro.net/123/imgs/https.png) 물리학백과: 불확정성원리(https://terms.naver.com/entry.naver?docId=5810582&cid=60217&categoryId=60217)
물리학백과: 불확정성원리(https://terms.naver.com/entry.naver?docId=5810582&cid=60217&categoryId=60217)![[https]](http://tomoyo.ivyro.net/123/imgs/https.png) 물리산책: 불확정성의 원리(https://terms.naver.com/entry.naver?docId=3568644&cid=58941&categoryId=58960)
물리산책: 불확정성의 원리(https://terms.naver.com/entry.naver?docId=3568644&cid=58941&categoryId=58960)https://everything2.com/title/Heisenberg Uncertainty Principle (long)