Difference between r1.15 and the current
@@ -144,8 +144,11 @@
[[반응지수,reaction_quotient]] Q----
[[WpKo:평형_상수]]
[[WpSp:Equilibrium_constant]]
[[WpEn:Equilibrium_constant]]
Up:
[[평형,equilibrium]]
[[화학평형,chemical_equilibrium]]
기호: 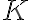
평형상태를 예측하게 해 줌.
해당 온도에서 반응이 어느 정도까지 생성물로 진행될지에 대한 척도.
해당 온도에서 반응이 어느 정도까지 생성물로 진행될지에 대한 척도.
2. 평형에 미치는 온도의 영향 ¶
온도만이 K를 변화시킬 수 있다.
열을 반응물이나 생성물 중 하나로 생각해 보자.
음의 ΔHr°을 가지는 계(발열반응)에서 온도의 상승은 K를 감소시킨다.
(엔탈피,enthalpy#s-6 표준반응엔탈피)
발열반응에서 열은 생성물이다.
흡열반응에서 열은 반응물이다.
양의 ΔHr°을 가지는 계(흡열반응)에서 온도의 상승은 K를 증가시킨다.흡열반응에서 열은 반응물이다.
음의 ΔHr°을 가지는 계(발열반응)에서 온도의 상승은 K를 감소시킨다.
(엔탈피,enthalpy#s-6 표준반응엔탈피)
3. 평형페이지에서 가져옴. TOMERGE ¶
{
예. 25 °C 에서 가역반응 N2O4(g) ⇄ 2NO2(g)에서 [NO₂]2 / [N₂O₄] 값은 4.63×10-3으로 거의 일정. 평형상수는
![$K=\frac{[\textrm{NO_2}]^2}{\textrm{[N_2O_4]}}=4.63\times 10^{-3}$ $K=\frac{[\textrm{NO_2}]^2}{\textrm{[N_2O_4]}}=4.63\times 10^{-3}$](/123/cgi-bin/mimetex.cgi?\Large K=\frac{[\textrm{NO_2}]^2}{\textrm{[N_2O_4]}}=4.63\times 10^{-3})
좀더 일반적으로, 반응
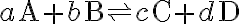
에서 평형상수는
![$K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$ $K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$](/123/cgi-bin/mimetex.cgi?\Large K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b})
}
4. tmp to mv.... 평형상수 K, 반응지수 Q 비교 ¶
이하 고딩 화II
평형상수 K
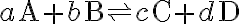 (a~d: 반응계수)
(a~d: 반응계수)
에서 평형상수 K는
![$K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$ $K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$](/123/cgi-bin/mimetex.cgi?\Large K=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b})
([A], [B], [C], [D]는 각각 A, B, C, D의 평형 농도(M))
// mv up
([A], [B], [C], [D]는 각각 A, B, C, D의 평형 농도(M))
반응지수 Q
![$Q=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$ $Q=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b}$](/123/cgi-bin/mimetex.cgi?\Large Q=\frac{[{\rm C}]^c [{\rm D}]^d}{[{\rm A}]^a [{\rm B}]^b})
([A], [B], [C], [D]는 각각 A, B, C, D의 현재 농도(M))
// fork to 반응지수,reaction_quotient
평형상수식에 반응물과 생성물의 현재농도(M)을 대입하여 구한 값
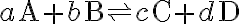 (a~d: 반응계수)
(a~d: 반응계수)
에서 반응지수 Q는([A], [B], [C], [D]는 각각 A, B, C, D의 현재 농도(M))
K, Q를 비교해 반응의 진행방향 예측
반응의 방향과 Q와 K의 상대적 크기
Q<K 정반응 우세, 오른쪽으로 진행
Q>K 역반응 우세, 왼쪽으로 진행
Q=K 평형
| Q<K | 정반응 우세 |
| Q=K | 평형 |
| Q>K | 역반응 우세 |
반응의 방향과 Q와 K의 상대적 크기
Q<K 정반응 우세, 오른쪽으로 진행
Q>K 역반응 우세, 왼쪽으로 진행
Q=K 평형
7. 물의 이온 곱 상수 Kw ¶
H2O(ℓ) + H2O(ℓ) ⇌ H3O+(aq) + OH-(aq)
![$K_c=\frac{\textrm{[H_3O^+][OH^-]}}{\textrm{[H_2O]^2}}$ $K_c=\frac{\textrm{[H_3O^+][OH^-]}}{\textrm{[H_2O]^2}}$](/123/cgi-bin/mimetex.cgi?\Large K_c=\frac{\textrm{[H_3O^+][OH^-]}}{\textrm{[H_2O]^2}})
물의 이온곱상수는
Kc[H2O]2 = Kw = [H3O+][OH-] = 1.0×10-14 (at 25°C)
Kc[H2O]2 = Kw = [H3O+][OH-] = 1.0×10-14 (at 25°C)
[H3O+]의 변화는 [OH-]를 반대로 변하게 한다.
| 산성 용액에서, | [H3O+] > [OH-] |
| 염기성 용액에서, | [H3O+] < [OH-] |
| 중성 용액에서, | [H3O+] = [OH-] |
ex. (54m)
물에 HCl을 녹여 [H3O+]=3.0×10-4 M이 되게 하였다. [OH-]를 계산하라. 이 용액은 산/중/염기성?
물에 HCl을 녹여 [H3O+]=3.0×10-4 M이 되게 하였다. [OH-]를 계산하라. 이 용액은 산/중/염기성?
sol.
Kw=1.0×10-14=[H3O+][OH-] 이므로
[OH-]=Kw/[H3O+]=1.0×10-14/3.0×10-4=3.3×10-11 M
3.0×10-4 M > 3.3×10-11 M
[H3O+] > [OH-]
따라서 산성이다.
Kw=1.0×10-14=[H3O+][OH-] 이므로
[OH-]=Kw/[H3O+]=1.0×10-14/3.0×10-4=3.3×10-11 M
3.0×10-4 M > 3.3×10-11 M
[H3O+] > [OH-]
따라서 산성이다.


![[https]](/123/imgs/https.png)