기호: 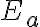
단위:
아레니우스_식,Arrhenius_equation
})
에 나타남.
Arrhenius equation의 로그 형태에서 Arrhenius plot을 그리고 그 기울기에서 활성화에너지를 얻을 수 있음. (해당 페이지 참조)
아레니우스_식,Arrhenius_equation
Arrhenius equation의 로그 형태에서 Arrhenius plot을 그리고 그 기울기에서 활성화에너지를 얻을 수 있음. (해당 페이지 참조)
화학반응,chemical_reaction은 반응물 원자간 결합이 끊어지고 다시 새로운 결합(화학결합,chemical_bond)을 형성하는 것이므로 결합을 끊으려면 일정한 에너지,energy가 필요한데, 이를 활성화에너지라고 함.
가역반응은 두 개의 활성화에너지를 가짐. (당연)

- 정반응의 활성화에너지
- 역반응의 활성화에너지

Up:

