Difference between r1.2 and the current
@@ -1,5 +1,33 @@
<<TableOfContents>>= 김민경 =
아레니우스 방정식
$k=Ae^{-\frac{E_a}{RT}}$
여기서
$k$ : 온도 T에서의 [[속도상수,rate_constant]]
$E_a$ : [[활성화에너지,activation_energy]]
$R$ : [[기체상수,gas_constant]]
$T$ : 절대 [[온도,temperature]]
$A$ : 충돌 빈도 인자 (분자 배향과 관계)
또는 잦음률(frequency factor)
$A=pZ$
$Z$ : 충돌빈도
$p$ : 배향 확률 인자
식을 적당히 변형하면 (쉽다)
$\ln k=\ln A-\frac{E_a}{RT}$
그리고 온도가 $T_1,T_2$ 인 두 경우를 생각한다. 이 때 속도상수가 $k_1,k_2$ 라고 둔다. 이 때 각각 다음 식이 성립. (칠판)
$T_1,k_1: \ln k_1 = \ln A-\frac{E_a}{RT_1}$
$T_2,k_2: \ln k_2 = \ln A-\frac{E_a}{RT_2}$
$\ln\frac{k_2}{k_1}=-\frac{E_a}{R}\left( \frac{1}{T_2}-\frac{1}{T_1} \right)$
바로 위 식은 외우지 않는다. 외우는 것은 첫 식만 외우고 두번째 식은 자연로그만 알면 변환할 수 있고 두 경우를 생각해 마지막 식을 유도한다. (위에 기록한 순서.)
from https://youtu.be/cBQ2yjw3rGc 19m
----
----$k_A(T)=Ae^{-E_a/RT}$ CHK
@@ -7,6 +35,12 @@
$E_a$ : [[활성화에너지,activation_energy]]$R$ : [[기체상수,gas_constant]]
$T$ : 절대온도
[[https://blog.naver.com/hafs_snu/220860685050 여기]]에 있는 이미지에
k : 반응에 기여한 초당 충돌수
A : 총 충돌수
e^^-E,,a,,/RT^^ : 충돌한 것 중에 반응한 것의 비율
이라는데 정말인가? CHK
----$k=Ae^{-E_{\rm a}/(RT)}$
@@ -25,7 +59,7 @@
> $k=pZe^{-E_a/RT}$> $k=Ae^{-E_a/RT}$
$k$ : 속도상수
$k$ : [[속도상수,rate_constant]]
$p$ : 반응하기에 적절한 배향을 가지는 충돌분율$Z$ : 충돌 빈도
$E_a$ : 활성화에너지
@@ -38,6 +72,11 @@
$\ln k = \left(\frac{-E_a}{R}\right) \left(\frac1T\right) + \ln A$
(1차함수 $y=mx+b$ 의 형태)
Arrhenius plot
이렇게 y축을 $\ln k,$ x축을 $1/T$ 로 그래프를 그린 것
[[기울기,slope]]에서 [[활성화에너지,activation_energy]]를 알 수 있음.
$E_a=-R\times(\textrm{slope})$
유도법
$k=Ae^{-E_a/RT}$
@@ -58,11 +97,11 @@
= 아레니우스 식의 두 점 형태 =$\ln\left(\frac{k_2}{k_1}\right)=\left(-\frac{E_a}{R}\right) \left(\frac1{T_2}-\frac1{T_1}\right)$
Masterton Ch11 summary 부분에 나온 같은 식은
$\ln\frac{k_2}{k_1}=\frac{E_a}{R}\left[\frac{1}{T_1}-\frac{1}{T_2}\right]$
Related: [[반응속도상수,reaction_rate_constant]]에도 관련 내용 있음
Related: [[속도상수,rate_constant]]에도 관련 내용 있음
----
Up: [[반응속도론,chemical_kinetics]]
Up: [[반응속도론,chemical_kinetics]] 에 충돌분율f, 입체인자p 섹션 있는데 합쳐야......TODO
1. 김민경 ¶
아레니우스 방정식
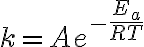
여기서
 : 온도 T에서의 속도상수,rate_constant
: 온도 T에서의 속도상수,rate_constant
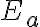 : 활성화에너지,activation_energy
: 활성화에너지,activation_energy
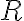 : 기체상수,gas_constant
: 기체상수,gas_constant
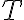 : 절대 온도,temperature
: 절대 온도,temperature
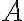 : 충돌 빈도 인자 (분자 배향과 관계)
: 충돌 빈도 인자 (분자 배향과 관계)
식을 적당히 변형하면 (쉽다)
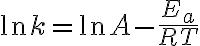
그리고 온도가 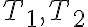 인 두 경우를 생각한다. 이 때 속도상수가
인 두 경우를 생각한다. 이 때 속도상수가 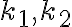 라고 둔다. 이 때 각각 다음 식이 성립. (칠판)
라고 둔다. 이 때 각각 다음 식이 성립. (칠판)
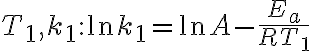
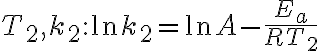
)
바로 위 식은 외우지 않는다. 외우는 것은 첫 식만 외우고 두번째 식은 자연로그만 알면 변환할 수 있고 두 경우를 생각해 마지막 식을 유도한다. (위에 기록한 순서.)
또는 잦음률(frequency factor)
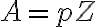
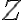 : 충돌빈도
: 충돌빈도
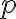 : 배향 확률 인자
: 배향 확률 인자
from https://youtu.be/cBQ2yjw3rGc 19m
A : 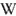 Pre-exponential_factor = A factor
Pre-exponential_factor = A factor
R : 기체상수
T : 절대온도
k : 반응속도상수(reaction rate constant or reaction rate coefficient)
R : 기체상수
T : 절대온도
k : 반응속도상수(reaction rate constant or reaction rate coefficient)
속도상수는 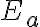 가 증가할 때 감소하고,
가 증가할 때 감소하고, 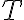 가 증가할 때 증가한다.
가 증가할 때 증가한다.
2. 아레니우스 식의 로그 형태 ¶
(1차함수
Arrhenius plot
이렇게 y축을 x축을
x축을 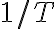 로 그래프를 그린 것
로 그래프를 그린 것
기울기,slope에서 활성화에너지,activation_energy를 알 수 있음.
)
유도법
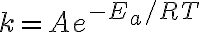
양변에 로그를 취하면
\frac1T+\ln A)
축 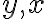 가 각각
가 각각 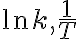 인 그래프, 감소하는 일차함수.
인 그래프, 감소하는 일차함수.
이렇게 y축을
기울기,slope에서 활성화에너지,activation_energy를 알 수 있음.
y절편은 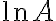
기울기는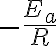
그래서 기울기에서 활성화에너지를 구할 수 있다.기울기는
두 다른 온도 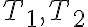 와 그 때의 속도상수
와 그 때의 속도상수 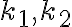 를 알고 있다면
를 알고 있다면
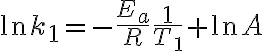

이렇게 연립방정식을 만들어서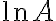 가 소거되므로 활성화에너지를 구할 수 있다.
가 소거되므로 활성화에너지를 구할 수 있다.
이렇게 연립방정식을 만들어서
3. 아레니우스 식의 두 점 형태 ¶
Masterton Ch11 summary 부분에 나온 같은 식은
![$\ln\frac{k_2}{k_1}=\frac{E_a}{R}\left[\frac{1}{T_1}-\frac{1}{T_2}\right]$ $\ln\frac{k_2}{k_1}=\frac{E_a}{R}\left[\frac{1}{T_1}-\frac{1}{T_2}\right]$](/123/cgi-bin/mimetex.cgi?\Large \ln\frac{k_2}{k_1}=\frac{E_a}{R}\left[\frac{1}{T_1}-\frac{1}{T_2}\right])
Related: 속도상수,rate_constant에도 관련 내용 있음
Up: 반응속도론,chemical_kinetics 에 충돌분율f, 입체인자p 섹션 있는데 합쳐야......TODO


![[https]](/123/imgs/https.png)