기호 H
'열함량' 정도
특정 온도와 압력에서, 어떤 물질이 가지는 고유한 에너지 함량
특정 온도,temperature와 압력,pressure에서, 어떤 물질,substance,matter이 가지는 고유한 에너지,energy 함량
특정 온도,temperature와 압력,pressure에서, 어떤 물질,substance,matter이 가지는 고유한 에너지,energy 함량
크기성질임 (소비된 반응물 양에 정비례)
정의:
엔탈피 변화 시 발열, 흡열
H = E + PV
엔탈피 = 내부에너지 + 압력 × 부피
H = U + PV
엔탈피(H)는 내부에너지(U)에 압력(P)와 부피(V)의 곱을 더한 것.
U : 내부에너지,internal_energy
밀접: 화학 반응에서의 열,heat엔탈피 = 내부에너지 + 압력 × 부피
H = U + PV
엔탈피(H)는 내부에너지(U)에 압력(P)와 부피(V)의 곱을 더한 것.
U : 내부에너지,internal_energy
엔탈피 변화 시 발열, 흡열
보통 직접 측정할 수 없고, 화학 반응에서 열의 변화(출입하는 열에너지)를 통해 간접적으로 측정
반응 엔탈피 (enthalpy of reaction) = 반응열 (heat of reaction) ΔH, ΔHrxn 반응열,heat_of_reaction
물의 융해 엔탈피 : 얼음이 녹음 : 열을 흡수 : ΔH융해 > 0
연료의 연소 엔탈피 : 열을 발생(방출) : ΔH연소 < 0
관련 반응을 명시해야 함 (단어 의미상 당연히)
ΔH < 0 : 반응이 흡열 반응임을 의미
정반응의 ΔH와 역반응의 ΔH는 크기는 같고 부호는 반대
쉬운 예물질 상태도 명시해야 함 (ex. 생성물이 (g)인지 (ℓ)인지에 따라 당연히 값이 달라짐)
ΔH < 0 : 반응이 발열 반응임을 의미ΔH < 0 : 반응이 흡열 반응임을 의미
정반응의 ΔH와 역반응의 ΔH는 크기는 같고 부호는 반대
물의 융해 엔탈피 : 얼음이 녹음 : 열을 흡수 : ΔH융해 > 0
연료의 연소 엔탈피 : 열을 발생(방출) : ΔH연소 < 0
주의할 점 ![[http]](/123/imgs/http.png) src
src
1. 엔탈피 값은 압력, 온도에 따라 다르다.
따라서 기준 상태를 정해주는 것이 중요하다. 표준상태란 1 atm, 25 °C 일 때를 말한다. 표준상태에서의 엔탈피를 표준엔탈피라 하고, H°로 표시한다.
![[http]](/123/imgs/http.png) src
src1. 엔탈피 값은 압력, 온도에 따라 다르다.
따라서 기준 상태를 정해주는 것이 중요하다. 표준상태란 1 atm, 25 °C 일 때를 말한다. 표준상태에서의 엔탈피를 표준엔탈피라 하고, H°로 표시한다.
2. 엔탈피는 상태함수이다.
(상태함수: 계가 특정 상태에 있으면 어떤 경로를 통해 그 상태에 도달하였는지 상관없는 성질)
(경로함수: 어떤 과정을 거치는지에 따라 값이 달라지는 성질)
참고로 열(q), 일(w)은 경로함수지만, 그 합인 내부에너지변화(ΔE)는 상태함수로서, 경로에 상관없이 같다.
(상태함수: 계가 특정 상태에 있으면 어떤 경로를 통해 그 상태에 도달하였는지 상관없는 성질)
(경로함수: 어떤 과정을 거치는지에 따라 값이 달라지는 성질)
참고로 열(q), 일(w)은 경로함수지만, 그 합인 내부에너지변화(ΔE)는 상태함수로서, 경로에 상관없이 같다.
3. 엔탈피는 세기성질이다.
(세기성질: 크기가 물질의 양에 비례하는 성질)
(크기성질: 물질의 양이 변해도 크기에 변화가 없는 성질 ex. 밀도)
(세기성질: 크기가 물질의 양에 비례하는 성질)
(크기성질: 물질의 양이 변해도 크기에 변화가 없는 성질 ex. 밀도)
ttttmp
http://www.sciencenanum.net/chemistry/condensed.html
http://www.sciencenanum.net/chemistry/thermochem.html
http://www.sciencenanum.net/chemistry/thermochem/thermochem_05.html
http://www.sciencenanum.net/chemistry/condensed.html
http://www.sciencenanum.net/chemistry/thermochem.html
http://www.sciencenanum.net/chemistry/thermochem/thermochem_05.html
1. from ebs; to merge ¶
엔탈피(H): 일정한 압력에서, 어떤 물질이 가지고 있는 고유한 총 에너지 함량
절대값을 정확하게 측정하는 것은 불가능하지만 반응열을 측정하면 물질이 가진 엔탈피의 차이를 알 수 있음
일정 압력에서 열의 출입은 엔탈피의 변화(ΔH)
반응열(Q): ΔH와 절대값은 같고 부호는 반대
반응엔탈피(ΔH)
= (생성물질의 총 엔탈피) - (반응물질의 총 엔탈피)
= ΣH(생성물질) - ΣH(반응물질)
생성엔탈피= ΣH(생성물질) - ΣH(반응물질)
: 어떤 물질 1몰이 성분 원소의 가장 안정한 원소로부터 생성될 때의 반응엔탈피
표준생성엔탈피: 1기압에서의 생성엔탈피
단위 kJ/mol다른 모든 enthalpy도 마찬가지??
반응엔탈피/분해엔탈피: 어떤 물질 1몰이 가장 안정한 성분 원소로 분해될 때의 반응엔탈피
생성엔탈피와 절대값 같고 부호 반대반응엔탈피/연소엔탈피
: 어떤 물질 1몰이 완전연소하여 가장 안정한 생성물이 될 때의 반응엔탈피
연소반응은 항상 발열반응이므로, 연소엔탈피(ΔH)는 항상 (-)값반응엔탈피/중화엔탈피
: 산의 H+(aq) 1몰과 염기의 OH-(aq) 1몰이 중화반응하여 1몰의 H2O(l)이 생성될 때의 반응엔탈피
중화엔탈피는 반응하는 산과 염기의 종류에 관계 없이 일정
related: 알짜이온반응식
반응엔탈피/용해엔탈피중화엔탈피는 반응하는 산과 염기의 종류에 관계 없이 일정
related: 알짜이온반응식
: 어떤 물질 1몰이 다량의 물에 용해될 때의 반응엔탈피
(EBS)2. from zum; to merge ¶
엔탈피
반응열 : 반응물의 엔탈피 합에서 생성물의 엔탈피 합을 뺀 값
Up: 열,heat
표준엔탈피 H°
반응열(Q)과 반응엔탈피(ΔH)25 ℃, 1기압에서의 엔탈피 값
반응엔탈피 ΔH일정한 압력에서, 화학 반응이 일어날 때의 엔탈피 변화
반응엔탈피 = 생성물의 엔탈피 합 - 반응물의 엔탈피 합
ΔH = ΣH생성물 - ΣH반응물
반응엔탈피 = 생성물의 엔탈피 합 - 반응물의 엔탈피 합
ΔH = ΣH생성물 - ΣH반응물
반응열 : 반응물의 엔탈피 합에서 생성물의 엔탈피 합을 뺀 값
Q = ΣH반응물 - ΣH생성물
반응열 = (반응물의 엔탈피 합) - (생성물의 엔탈피 합)
일정한 압력에서, 반응열(Q)과 반응엔탈피(ΔH)는 부호 반대임반응열 = (반응물의 엔탈피 합) - (생성물의 엔탈피 합)
Q = -ΔH
| 반응열 | 반응엔탈피 | |||
| 발열반응 | Q>0 | ΔH<0 | 반응물보다 생성물이 더 안정함 | 주위 온도가 올라감 |
| 흡열반응 | Q<0 | ΔH>0 | 생성물보다 반응물이 더 안정함 | 주위 온도가 내려감 |
4. 엔탈피 변화 (AKA 반응엔탈피) ΔH ¶
엔탈피 변화(ΔH) = (생성 물질의 엔탈피) - (반응 물질의 엔탈피)
ΔH = ΔE + Δ(PV)
P-V일 이외의 다른 일이 관여하지 않는다면 ΔE = Q - PΔV이므로
ΔH = Q + VΔP
여기서 Δ(PV) = (PΔV + VΔP) 이므로,
ΔH = ΔE + PΔV + VΔP - how? CHKP-V일 이외의 다른 일이 관여하지 않는다면 ΔE = Q - PΔV이므로
ΔH = Q + VΔP
관련: 헤스_법칙,Hess_s_law
반응엔탈피(ΔH) = 엔탈피변화(ΔH)
= (생성물의 엔탈피 합) - (반응물의 엔탈피 합)
= ΣH생성물 - ΣH반응물
= ΣH생성물 - ΣH반응물
| 발열 반응 | 발열과정 exothermic | ΣH반응물 > ΣH생성물 | ΔH<0 | 계의 엔탈피 감소 | 주위의 엔탈피 증가 |
| 흡열 반응 | 흡열과정 endothermic | ΣH반응물 < ΣH생성물 | ΔH>0 | 계의 엔탈피 증가 | 주위의 엔탈피 감소 |
6. 표준 반응 엔탈피 ΔH°r ¶
ΔH°r
1기압 하에서 일어나는 반응의 엔탈피 변화량
1기압 하에서 일어나는 반응의 엔탈피 변화량
표준 반응 엔탈피 = (생성물의 표준 생성 엔탈피 합) - (반응물의 표준 생성 엔탈피 합)
7. 표준 생성 엔탈피 (AKA 표준생성열) standard enthalpy of formation ΔH°f ¶
기호: 여기서 문자를 위아래로 wiki syntax로 쓰는 방법이 없는데 ( 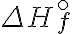 는 되지만 )
는 되지만 )
ΔH°f 인가,
ΔHf° 인가?
°(degree)인가 0(superscript zero)인가?
ΔH°f 인가,
ΔHf° 인가?
°(degree)인가 0(superscript zero)인가?
1기압에서 어떤 화합물 1몰이 그 화합물을 구성하고 있는 성분 원소의 가장 안정한 상태에서 생성될 때의 반응 엔탈피
1 atm에서, 각 원소로부터 1 mol의 화합물을 생성할 때 열의 변화
- °: 표준상태(1 atm)의 조건이라는 뜻
- f: 생성(formation)을 뜻함
엔탈피 표현식에서 기준점(0 kJ/mol) 역할을 하는듯..........CHK
ΔHf°(C, 흑연) = 0
ΔHf°(C, 다이아몬드) = 1.90 kJ/mol
ΔHf°(C, 다이아몬드) = 1.90 kJ/mol
ΔH반응° = ΣΔHf°(생성물) - ΣΔHf°(반응물)
ex. 반응식이 a A + b B → c C + d D 일 경우
ΔH반응° = (c ΔHf°(C) + d ΔHf°(D)) - (a ΔHf°(A) + b ΔHf°(B))
ΔH반응° = (c ΔHf°(C) + d ΔHf°(D)) - (a ΔHf°(A) + b ΔHf°(B))
7.1. ΔHf°를 구하는 두 방법 ¶
1. 직접법
: 원소로부터 쉽게 합성할 수 있는 화합물의 반응 엔탈피에서 구함
: 원소로부터 쉽게 합성할 수 있는 화합물의 반응 엔탈피에서 구함
ex. 이산화탄소의 생성엔탈피는, 표준상태 흑연과 산소분자가 표준상태의 이산화탄소로 될 때의 반응엔탈피
C(흑연) + O2(g) → CO2(g) ..... ΔH반응° = -393.5 kJ/mol
ΔHf°(C, 흑연) = ΔHf°(O2, g) = 0 (이 둘은 안정하므로)
ΔH반응° = ΔHf°(CO2, g) - (ΔHf°(C, 흑연) + ΔHf°(O2, g)) = -393.5 kJ/mol
ΔHf°(CO2, g) = -393.5 kJ/mol
ΔHf°(C, 흑연) = ΔHf°(O2, g) = 0 (이 둘은 안정하므로)
ΔH반응° = ΔHf°(CO2, g) - (ΔHf°(C, 흑연) + ΔHf°(O2, g)) = -393.5 kJ/mol
ΔHf°(CO2, g) = -393.5 kJ/mol
.......너무 잡다한 것을 적은 듯..........
2. 간접법
: 많은 화합물은 원소로부터 직접 합성 불가: 헤스의 법칙으로 계산
: 많은 화합물은 원소로부터 직접 합성 불가: 헤스의 법칙으로 계산
See 헤스_법칙,Hess_s_law
8. 결합엔탈피 bond enthalpy ¶
BE, ΔHB
기체상에서 결합 1몰이 끊어질 때 일어나는 엔탈피의 변화 CHK
기체상에서 결합 1몰을 끊기 위해 필요한 에너지 = 결합 해리 에너지
기체상에서 결합 1몰을 끊기 위해 필요한 에너지 = 결합 해리 에너지
기체 분자 1 mol에서, 특정 결합을 끊을 때 필요한 엔탈피 변화량
H2(g) → H(g) + H(g) .... ΔH° = 436.4 kJ
H2(g) → H(g) + H(g) .... ΔH° = 436.4 kJ
결합엔탈피는
단일결합 < 이중결합 < 삼중결합
평균결합엔탈피 (다원자 분자 결합에 대해) 가 있음반응엔탈피를 평균결합엔탈피로 추정 가능
ΔH° = Σ BE(반응물) - Σ BE(생성물)
= (투입된 전체 에너지) - (방출한 전체 에너지)
9. 반응엔탈피 enthalpy of reaction ¶
반응열과 같은건가 아님 부호반대인가??????
기호: ΔH, ΔHrxn (rxn = reaction)
반응엔탈피 = ΣH생성물 - ΣH반응물
ΔH = 일정 압력 하에서 반응 중에 방출하거나 흡수하는 열
흡열반응
0 °C, 1 atm에서 얼음 1 mol이 녹아 물이 될때
0 °C, 1 atm에서 얼음 1 mol이 녹아 물이 될때
H2O(s) → H2O(l)
ΔH = 6.01 kJ/mol
(계가 열을 흡수) = (흡열) = (ΔH > 0)ΔH = 6.01 kJ/mol
발열반응
0 °C, 1 atm에서 물 1 mol이 얼음이 될때
0 °C, 1 atm에서 물 1 mol이 얼음이 될때
H2O(l) → H2O(s)
ΔH = -6.01 kJ/mol
(계가 열을 방출) = (발열) = (ΔH < 0)ΔH = -6.01 kJ/mol
다음 반응물/생성물 앞뒤가 반대임에 주의!
결합에너지로 구하는 방법
ΔH반응 = Σ 반응물결합E - Σ 생성물결합E
표준생성엔탈피로 구하는 방법ΔH반응 = Σ ΔHf°(생성물) - Σ ΔHf°(반응물)
from https://youtu.be/E0UobzUe8Jc 30m어원: 그리스어 enthalpein(따뜻하게 함)에서

